Thérapie Génique
English version below
Thérapie génique par AAV de la rétinite pigmentaire 28 (RP28) associée au gène FAM161A
La rétinite pigmentaire (RP) est une maladie dégénérative de la rétine dont l’incidence est de 1:4000 dans le monde. Cette dystrophie des bâtonnets et de cônes évolue lentement vers la cécité et aucun traitement efficace n’est actuellement disponible. Parmi les cas de RP, la RP28 est une ciliopathie affectant uniquement l’œil qui a été associée à des mutations récessives du gène humain FAM161A dans plusieurs populations ethniques (Bandah-Rozenfeld et al. 2010, Langmann et al. 2010). L’expression de la protéine FAM161A a été observée dans le cil connecteur du photorécepteur (réf) et nous avons ensuite démontré, en collaboration avec le laboratoire de Paul Guichard et Virginie Hamel (UNIGE), que la protéine FAM161A appartient à la structure d’échafaudage interne du cil connecteur du photorécepteur de souris (Mercey et al. 2022).
La souris déficiente pour Fam161Atmb/tmbmise au point par nos collègues Avigail Beryozkin et Dror Sharon (Hadassah Medical Center) reproduit la progression de la maladie humaine (Beryozkin et al. 2021). Nous avons démontré l’amélioration de la survie et de la fonction des photorécepteurs dans le modèle de souris Fam161Atmb/tmbpar l’administration sous-rétinienne d’un vecteur de virus adéno-associé (AAV), qui code pour l’ADNc long de Fam161A (Matsevich et al. 2023). En transposant cette approche avec le gène FAM161A humain, il a été observé que seule la co-injection de deux vecteurs AAVs, qui délivrent à la fois les isoformes longue et courte humaines, permettait de sauver la fonction rétinienne de la souris Fam161Atmb/tmb. En outre, un niveau d’expression approprié est nécessaire, ce que nous avons obtenu grâce à l’utilisation d’une nouvelle séquence régulatrice dérivée du gène humain FAM161A (Arsenijevic et al. 2024). Nous continuons d’étudier de la fonction de FAM161A et d’évaluer des vecteurs AAV pour transférer cette stratégie de remplacement de gène vers une application clinique future.
Transfert de gène effectué par vecteur lentiviral pour les Amauroses de Leber causées par une déficience de RPE65
L’amaurose congénitale de Leber (ACL), la dystrophie rétinienne héréditaire enfantine la plus précoce et la plus sévère, est la cause principale de cécité chez les enfants. 10-15% des patients souffrant d’ACL portent une mutation du gène RPE65.
Nos chercheurs poursuivent une étude pré-clinique de transfert du gène sain RPE65 dans des modèles d’amaurose congénitale de Leber (ACL) de souris grâce à des injections sous-rétiniennes de vecteurs lentiviraux.
L’originalité de leur travail a été de définir une fenêtre thérapeutique précise ainsi que l’effet du transfert de gène RPE65 sur les cônes, la population de photorécepteurs la plus rapidement touchée dans ce modèle. Grâce à des mesures par électrorétinogramme (ERG) de bonnes réponses rétiniennes ont été obtenues dans des souris RPE65-/- traitées précocement (à 5 jours de vie) avec un vecteur lentiviral transférant le gène RPE65 (Bemelmans et al., 2006).
L’amélioration de la fonction des cônes a peu être démontrée. La sauvegarde de ces cellules a aussi été observée par des analyses histologiques.
Cependant ces mêmes cônes ne sont pas protégés quand le traitement est appliqué aux jeunes souris adultes (à 1 mois) démontrant une limite temporelle pour une préservation efficace. La moitié des patients portant une mutation RPE65 n’ont pas forcément une perte totale de la fonction de cette protéine ce qui peut avoir une conséquence sur le développement de la pathologie et donc sur la fenêtre thérapeutique.
Cette approche a été répétée sur un modèle de souris portant une mutation faux-sens retrouvée chez certains patients (R91W) (samardzija et al 2008). Dans ce modèle, la dégénérescence des cônes est retardée car il y a un reste d’expression de la protéine RPE65. Les mêmes types d’analyses cités ci-dessus ont révélé une sauvegarde partielle des cônes après un traitement à 1 mois d’âge (Kostic et al 2011). Non seulement le nombre de cônes répertoriés à l’âge du traitement est maintenu, mais 20% de plus de cônes (par rapport au nombre total dans la rétine de la souris saine) sont « rajeunis ». En effet, ce résultat suggère qu’une partie de la population des cônes n’exprime plus ses protéines spécifiques à ce stade (S-opsin, GNAT2) et ces cellules survivent comme des « fantômes » prêtes à récupérer leurs caractéristiques si un traitement adéquat est appliqué.
Nous avons ensuite évalué la sécurité d’une production de vecteurs de type GMP dans des conditions similaires à celles requises pour les essais cliniques mais avec une seule application topique de pommade dexaméthasone/oxytétracycline et sans anti-inflammatoire avant l’injection (Matet et al. 2017). Cette étude montre l’absence de détection des vecteurs en dehors du compartiment oculaire et une tolérance limitée au LV après la voie d’administration sous-rétinienne, ce qui suggère le besoin transitoire d’anti-inflammatoires pour contrecarrer les effets secondaires de l’inflammation comme cela est habituellement appliqué pour d’autres vecteurs viraux. Nous avons enfin démontré que notre vecteur peut augmenter le niveau de l’ARNm de RPE65 dans les cellules de l’épithelium pigmentaire dérivées d’iPSCs humaines (Udry et al. 2020), ce qui soutient fortement le potentiel de ce vecteur pour les applications cliniques de l’expression de gènes dans l’épithélium pigmentaire.
Développement de vecteurs lentiviraux pour la thérapie génique oculaire
La plupart des dégénérescences rétiniennes sont une conséquence du mauvais fonctionnement des photorécepteurs ou de l’épithélium pigmentaire ce qui nous a amené à définir les outils appropriés pour cibler spécifiquement ces types cellulaires.
Une base de l’approche par thérapie génique est d’atteindre le tissu ou la cellule approprié(e) de manière spécifique afin d’éviter des effets secondaires indésirables. Cette spécificité peut être déterminée par un tropisme limité du vecteur, par une fonction spécifique restreinte à un type cellulaire particulier ou par une expression spécifique déterminée par le choix du promoteur.
Cette dernière possibilité a été sélectionnée et nos chercheurs ont examiné l’activité de différents promoteurs dans la rétine murine après transfert de gène grâce à des vecteurs lentiviraux (Kostic et al., 2003). Ils ont aussi montré que la diffusion limitée de ces vecteurs dans l’espace sous-rétinien est due à une barrière physique entre les photorécepteurs et l’épithélium pigmentaire qui peut être altérée par l’utilisation de certains enzymes (Grüter et al., 2005). De plus, ils ont observé que le ciblage des vecteurs lentiviraux dépend du stade de la progression de la maladie (Calame et al 2011). Notamment les vecteurs lentiviraux pseudotypés avec l’enveloppe Mokola ciblent efficacement les cellules de Müller en cas de gliose dans le modèle murin Rho-/-. (Calame et al 2011).
Nos chercheurs poursuivent des études pour améliorer le transfert de gène dans la rétine grâce aux vecteurs lentiviraux.
Modèles pathologiques :
Un modèle de porc pour la dystrophie des cônes :
La compréhension des mécanismes de pathologie est cruciale pour les chercheurs qui veulent développer des nouvelles voies thérapeutiques. Des avancées majeures sont possibles grâce à des modèles animaux qui reproduisent des pathologies humaines. A cause des différences intrinsèques entre les organismes les limitations de ce genre de modèles doivent être prises en compte pour chaque maladie.
Dans ce contexte, les rongeurs sont une espèce limitée pour modéliser les maladies affectant les cônes chez les humains. En effet la distribution et l’organisation de ce type de photorécepteur sont adaptées à la vision de jour chez les primates tandis qu’il est adapté à la vision nocturne pour les rongeurs. Il est donc préférable d’étudier les déficiences visuelles liées aux cônes chez des animaux avec une région de la rétine enrichie en cônes et une taille d’œil similaire à l’homme. Les porcs qui ont en plus un taux élevé de reproduction conviennent donc particulièrement bien à ce genre de recherche.
La technique de transgénèse par vecteur lentiviral a été utilisée pour exprimer un allèle dominant du gène GUCY2D dans la rétine de porc et servir de modèle de la maladie CORD6 (Kostic et al. 2013). La caractérisation des porcs GUCY2DE837D/R838S a révélé un impact fonctionnel sur la vision ainsi que des modifications structurelles de la rétine. Des anormalités ont été détectées à l’âge de 11 semaines avec une progression lente dans l’année suivante. Une grande variété de sévérités a été constatée parmi les animaux porteurs de la mutation, d’une absence totale de symptôme à un grand déficit de fonction rétinienne.
Cette observation est particulièrement intéressante car elle imite la large hétérogénéité de sévérités décrites chez les patients CORD6 humains. Cette hétérogénéité trouvée chez les porcs est en accord avec la nature unique de chaque animal généré avec cette technique de vecteur lentiviral: le nombre de copies et les sites d’intégration du vecteur propres à chaque individu offrent la possibilité de créer un large échantillonnage d’animaux qui ont en commun la signature pathologique due à la mutation.
Cette diversité confirme l’effet pathologique de l’allèle et peut aider à identifier les facteurs intrinsèques et environnementaux impliqués dans la pénétrance. L’efficacité de cette technique a ainsi démontré le potentiel de cette stratégie pour générer des modèles de pathologie humaine et l’implication de la mutation de GUCY2D dans la dystrophie de cônes CORD6 (Kostic et al. 2013).
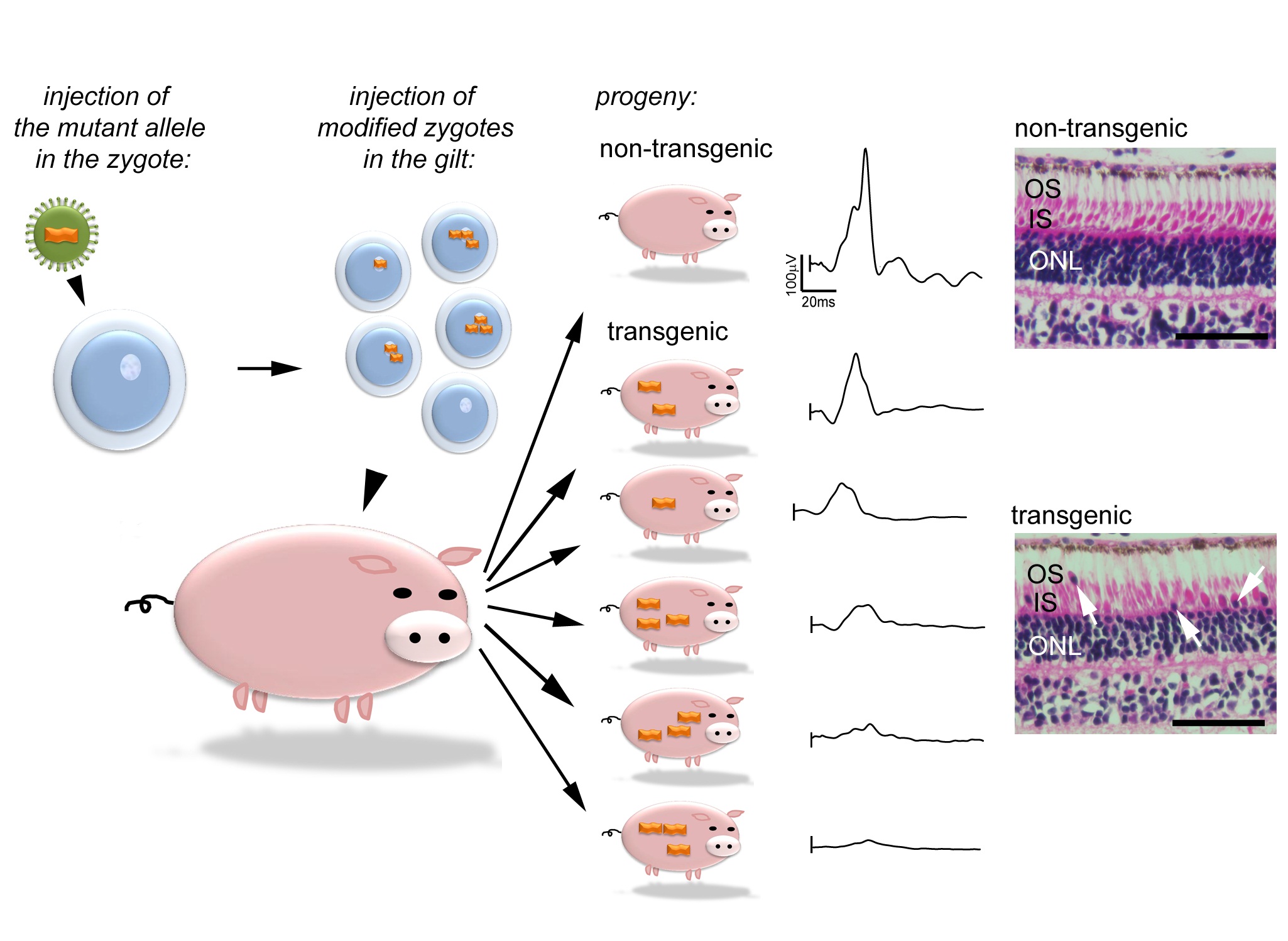
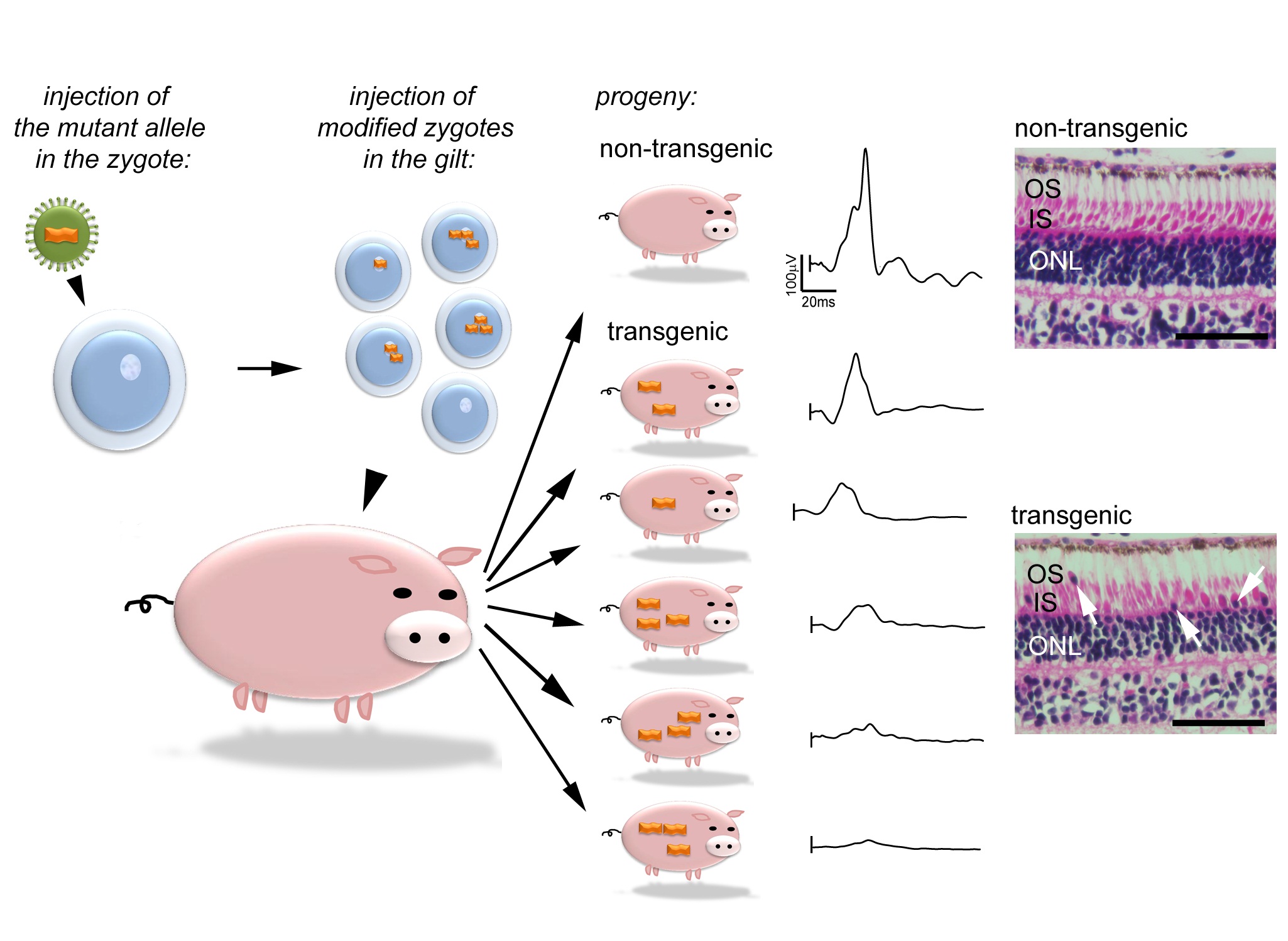
Figure – Illustration de la genèse d’un modèle de porc pour la dystrophie des cônes. Les particules de vecteur lentiviral sont injectées dans l’espace périvitellin des zygotes pour transférer l’allèle mutant (trait orange) dans le génome du porc. Les zygotes manipulés sont ensuite transférés dans l’oviducte de truies préparées qui mettent bas des individus uniques de par leur nombre de copies du transgène et du site d’intégration. La caractérisation fonctionnelle (enregistrement des réponses rétiniennes) et morphologique (histologie) des animaux confirme que le groupe présente une large variété d’altérations de la réponse rétinienne mais tous ont un nombre plus élevé de noyaux cellulaires déplacés dans la couche des segments externes (flèches) comparé aux animaux contrôles. OS: segments externes des photorécepteurs; IS: segments internes des photorécepteurs; ONL: noyaux des photorécepteurs.
Gene Therapy
AAV-mediated gene therapy for FAM161A-associated retinitis pigmentosa 28 (RP28)
Retinitis Pigmentosa (RP) is a hereditary degenerative disease of the retina with an incidence of 1:4000 worldwide. This rod-cone dystrophy slowly often evolves into blindness and currently, no effective cure is available. Among RP cases, RP28 is a ciliopathy affecting uniquely the eye that has been associated with recessive mutations in the human FAM161A gene in several ethnic populations (Bandah-Rozenfeld et al. 2010, Langmann et al. 2010). Expression of the FAM161A protein was observed in the photoreceptor connecting (ref) and we have further demonstrated, in collaboration with Paul Guichard and Virginie Hamel’s lab (UNIGE), that FAM161A protein is belonging to the inner scaffold structure of the connecting cilium of mouse photoreceptor (Mercey et al. 2022). The Fam161Atmb/tmbdeficient mouse engineered by our colleagues Avigail Beryozkin and Dror Sharon (Hadassah Medical Center) replicates the progression of the human disease (Beryozkin et al. 2021). We have demonstrated the successful improvement of photoreceptor survival and function in the Fam161Atmb/tmbdeficient mouse model through the subretinal delivery of adeno-associated virus (AAV) vector, which encodes for the mouse long Fam161A cDNA (Matsevich et al. 2023). Upon translating this approach with the human FAM161A gene, it was observed that only the co-injection of two AAV vectors, which deliver both the human long and short isoforms, resulted in the rescue of Fam161Atmb/tmbmouse retinal function. Furthermore, an appropriate level of expression is required, which we achieved through the use of a novel regulatory sequence derived from the human FAM161A gene (Arsenijevic et al. 2024).We are currently engaged in further studies of FAM161A function and in the evaluating of AAV vectors for the translation of this gene replacement strategy to treat FAM161A deficiency.
Lentiviral-mediated gene transfer for RPE65-derived Leber congenital amaurosis
Leber congenital amaurosis (LCA) is an autosomal recessive childhood-onset retinal dystrophy where RPE65 mutations account for 10-15% of the cases (Gu et al., 1997; Marlhens et al., 1997). We are pursuing a preclinical study for treatment of LCA by lentiviral-mediated gene transfer of RPE65 in different mice models for LCA.
We defined a precise therapeutic window and the effect of gene transfer on cone photoreceptors in RPE65-deficient murine models. We were able to obtain a good electroretinogram (ERG) response in RPE65 -/- mice treated at postnatal day 5 with a lentiviral vector expressing RPE65 (Bemelmans et al. 2006). We also demonstrated preservation of cone function and survival up to 4 months after treatment. However cones were not protected when the treatment was applied in young adults (1 month of age) revealing the limited therapeutic window for cone rescue (Bemelmans et al. 2006).
Considering that half of RPE65 patients have a missense mutation which may lead to only partial loss of function, we evaluated the therapeutic window in the knock-in mouse model bearing the R91W mutation found in patients (Samardzija et al. 2008). In this model, the cone degeneration is delayed due to residual protein activity. Consistently, injections at 1 month of age partially rescue cones at the site of injection (Kostic et al. 2011). More interestingly, not only did the gene transfer maintain the number of cones surviving at the time of injection, but it also rejuvenated 20% more cone cells, that re-express cone markers (Kostic et al. 2011). This result suggests that a portion of cone cells are surviving as “ghost” cells which lack expression of several cone-specific proteins (such as S-opsin, GNAT2) but are able to be rehabilitated.
We then evaluated the safety of a GMP-like vector production under conditions similar to those required for clinical trials but with a single topical application of dexamethasone/oxytetracycline ointment and no anti-inflammatory agents prior injection (Matet et al. 2017). This study shows absence of detection of the vectors outside the ocular compartment and a limited tolerance for LV after subretinal administration route, which suggests the transient need of anti-inflammatory drugs to counteract the inflammation side effects as is usually applied for other viral vectors. We finally demonstrated that our vector can increase the level of RPE65 mRNA in human iPSCs-derived RPE cells (Udry et al. 2020) strongly supporting the potential of this vector for clinical applications of gene expression in the RPE.
Development of lentiviral vectors as a tool for gene therapy in the eye
Most retina degeneration disorders are due to photoreceptor or RPE dysfunction, which prompted us to define appropriate tools to specifically attain these cells.
One basis of gene therapy approach is to target the appropriate tissue or cells, allowing specific expression of the therapeutic gene where it is supposed to act as well as avoiding damaging secondary effects. This specificity can be determined at different levels: the vector may have a limited tropism, the transgene may have a specific function restricted to a defined cell type, or the promoter may lead to cell- or tissue-specific expression.
We chose to work on the latter possibility and to examine expression of different promoters in mouse retina using lentiviral vector delivery (Kostic et al. 2003). We showed that the limited diffusion of the vectors is due to a physical barrier present between photoreceptors and RPE (Grüter et al. 2005). Moreover we revealed that targeting of the lentiviral vector also depends on the progression of the disease (Calame et al. 2011). Notably, lentiviral vectors pseudotyped with the Mokola envelope efficiently reach Müller cells during the gliosis observed in the Rho-/- mouse model (Calame et al. 2011).
We are pursuing studies to enhance lentiviral diffusion and transduction in the mouse retina in order to optimize gene transfer in different animal models.
Disease models:
A pig model for cone dystrophy
The understanding of disease mechanisms is a key factor for many biomedical researchers who dedicate their work to the development of novel therapies. Major advances have been made using animal models that reproduce human diseases. Due to the intrinsic differences between organisms, limitations of these types of models have to be considered and should be evaluated for each specific disease.
In this context, rodents have a restricted similarity to humans in the case of retinal diseases affecting cone photoreceptors. Indeed the relative distribution and organization of this type of cells in primates are particularly suited to daylight vision compared to rodents which are adapted to a nocturnal lifestyle. It would be preferable to study cone deficiency in animals that have both a cone-enriched region of the retina and an eye size that is comparable to the human. Pigs fit into this niche, and deliver a numerous progeny which is an obvious advantage for research.
Lentiviral-mediated transgenesis was used to express a GUCY2D dominant allele in the retina in order to model the CORD6 disease (Kostic et al. 2013). Characterization of the GUCY2DE837D/R838S transgenic pigs revealed a functional impact on vision as well as retinal structure alterations. Abnormalities were observed at 11 weeks of age, with subsequent slow disease progression during the first year follow-up. Importantly a wide range of severities was found among the transgenic animals, from absence of physiological perturbation to strong retinal function deficit.
This is of particular relevance as it mimics the phenotypic range described in the human population. The range observed in pigs is consistent with the unique nature of each animal generated by lentiviral-directed transgenesis; both the number of copies of the transgene and the genomic integration sites are thought to lead to a panel of transgenic animals among which the common pathological features are the signature of the dominant mutant allele. Such diversity confirms the pathological effect of the transgene and may help to identify intrinsic and environmental factors involved in the mutation penetrance. Together with the efficacy of this technique, our study reveals the potential of such strategy to efficiently generate a large cohort of transgenic animals modeling a human disease and demonstrates that dominant mutations in the GUCY2D gene are responsible for cone function loss (Kostic et al. 2013).